Содержание
Аннотация
В открытое сравнительное интервенционное исследование было включено 54 пациента с хронической сердечной недостаточностью (ХСН) II функционального класса с сохраненной фракцией выброса (ФВ) левого желудочка (ЛЖ). Целью исследования являлась оценка динамики клинических, лабораторных и эхокардиографических показателей на фоне комплексного медикаментозного лечения у пациентов с ХСН с сохраненной ФВ ЛЖ старшего возраста. Основную группу составили 29 пациентов в возрасте 76 (73; 80) лет, принимавших Фозинап в дозе 15,9 ± 5,0 мг/сут, группу сравнения – 25 пациентов в возрасте 74 (71; 80) лет, принимавших эналаприл в дозе 16,4 ± 4,9 мг/сут. Проводился общепринятый физикальный осмотр, эхокардиография с расчетом индекса глобальной функции (ИГФ) ЛЖ. Включение в комплексную терапию препарата Фозинап способствовало улучшению клинического состояния пациентов основной группы в виде снижения на 1,7 балла (p < 0,001) показателя по шкале оценки клинического состояния, лучшему контролю диастолического (снижение на 5,4 ± 11,3 мм рт. ст.; р=0,019) и систолического (снижение на 10,8 ± 17,2 мм рт. ст.; р=0,003) артериального давления, что не наблюдалось в группе сравнения. Изменений скорости клубочковой фильтрации, а также уровня калия как в основной группе, так и в группе сравнения не было выявлено.
В группе сравнения ИГФ ЛЖ снизился на 3,3% (p = 0,006), ФВ ЛЖ – на 4,9%; p = 0,014 через 6 мес от начала терапии; в основной группе динамики ИГФ ЛЖ и ФВ ЛЖ не было. Эффективность и хорошая переносимость Фозинапа в составе комплексной терапии позволяют рассматривать его в качестве препарата выбора при лечении амбулаторных мультиморбидных пациентов старшего возраста с ХСН II функционального класса с сохраненной ФВ ЛЖ. Ключевые слова: фозиноприл, Фозинап, хроническая сердечная недостаточность, сохраненная фракция выброса левого желудочка.
Введение
Хроническая сердечная недостаточность (ХСН) – одно из распространенных осложнений большинства сердечно-сосудистых заболеваний, сопряженное с высоким уровнем госпитализаций и риском смерти. На сегодняшний день выделены предикторы летального исхода лиц с ХСН, в число которых входит старший возраст. Ежегодная частота госпитализаций в группе пациентов старшего возраста достигает 31,9%, коэффициент смертности составляет 7,2% [1, 2].
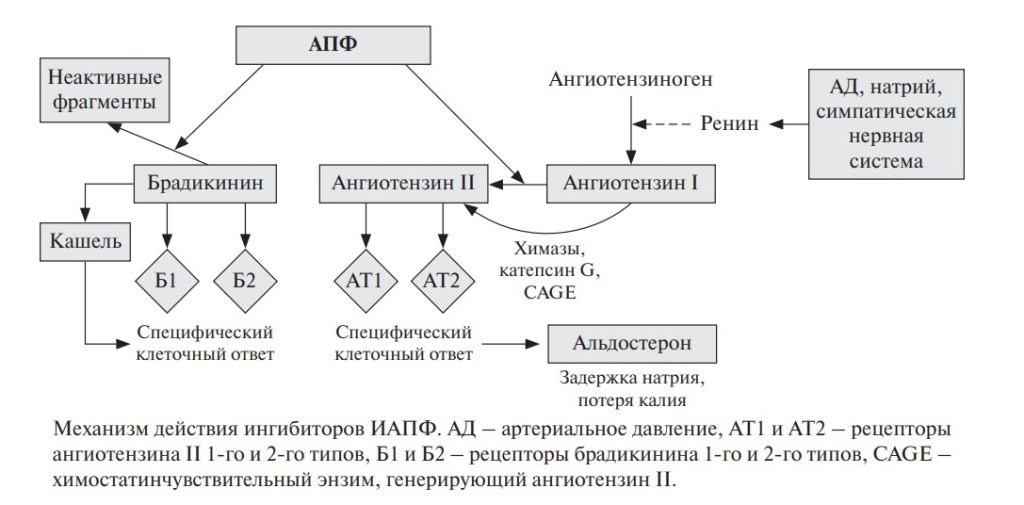
Механизм действия ингибиторов ИАПФ. АД – артериальное давление, АТ1 и АТ2 – рецепторы ангиотензина II 1-го и 2-го типов, Б1 и Б2 – рецепторы брадикинина 1-го и 2-го типов, CAGE – химостатинчувствительный энзим, генерирующий ангиотензин ІІ.
В последнее время качественно изменились подходы к диагностике и лечению пациентов с ХСН, что обусловлено выделением фенотипов в зависимости от фракции выброса (ФВ) левого желудочка (ЛЖ), существенными достижениями фармакотерапии и ориентацией на лечение заболеваний с высокой медико-социальной значимостью, при которых риск развития и прогрессирования ХСН максимально велик. Частота встречаемости ХСН с сохраненной ФВ ЛЖ (ХСНсФВ) в мировой популяции составляет 1–2% (примерно 32 млн. человек), увеличиваясь с возрастом пациентов. Однолетняя летальность пациентов с ХСНсФВ находится в пределах от 15 до 30%, в течение 5 лет наблюдения летальный исход регистрируется в 53–74% случаев [3]. Средняя частота госпитализаций составляет 1,4 раза в год [3, 4]. Мировое медицинское сообщество придерживается мнения, что ингибиторы ангиотензинпревращающего фермента (ИАПФ) при ХСНсФВ можно рассматривать в качестве препаратов выбора, в связи с накопленной большой доказательной базой в отношении улучшения прогноза у пациентов с артериальной гипертонией (АГ), ХСН и низкой ФВ ЛЖ, диабетической нефропатией, ведущая роль в патогенезе которых отводится чрезмерной активации ренин-ангиотензин-альдостероновой системы. Механизм действия ИАПФ основан на блокаде ангиотензинпревращающего фермента (АПФ), ответственного за превращение ангиотензина I в ангиотензин II, а также за деградацию нескольких гемодинамически активных пептидов, включая брадикинин, и отличается от механизма действия антагонистов рецепторов ангиотензина II, которые непосредственно подавляют активность рецепторов ангиотензина II 1-го типа, в то время как клиническая значимость стимуляции рецепторов 2-го типа не была подтверждена у людей (рисунок) [5, 6].
Первый ИАПФ тепротид был создан в 1971 г. в лаборатории фирмы Squibb (США). Препарат был синтезирован из яда гремучей змеи Bothrops jararaca, но из-за высокой токсичности, кратковременности действия, внутривенного пути введения не получил распространения в клинической практике. D.W. Cushman, M.A. Ondetti в 1975 г. в той же лаборатории синтезировали каптоприл – первый препарат для перорального применения [7]. В настоящее время создано около 50 препаратов группы ИАПФ, показания к применению которых постоянно расширяются. В конце ХХ века группой исследователей под руководством D.W. Cushman был синтезирован фозиноприл, запатентованный в 1980 г. и одобренный для медицинского применения в 1991 г. [8].
В последнее время активно изучаются возможности воспроизведенных копий (дженерики) оригинальных препаратов, содержащих аналогичную фармацевтическую субстанцию в такой же лекарственной форме, что и оригинальный препарат, и поступающие в обращение после оригинального лекарственного средства. С 2004 г. дженерик (Директива 2004/27/ЕС о внесении изменений в Директиву 2001/83/ЕС) рассматривается в качестве альтернативы патентованному препарату. Фозинап (ЗАО “Канонфарма продакшн”, Россия) является препаратом ИАПФ фозиноприла, содержащего фосфинильную группу. Фозиноприл – это каскадное пролекарство, которое действует после трансформации в печени и всасывания в слизистой оболочке желудочно-кишечного тракта (ЖКТ) с превращением в активный метаболит фозиноприлат, благодаря чему обеспечивается значительный органопротективный эффект. Сбалансированный двойной путь выведения из организма – почечная экскреция с мочой и выведение с желчью через ЖКТ – позволяет рассматривать фозиноприл в качестве препарата выбора у лиц старшего возраста и при сопутствующей патологии органов выделительной системы [9, 10].
Особый интерес представляет изучение эффективности и безопасности применения Фозинапа в составе медикаментозной
терапии
у амбулаторных пациентов с ХСНсФВ старшего возраста.
Целью исследования являлась оценка динамики клинических, лабораторных и эхокардиографических показателей на фоне
комплексного медикаментозного лечения у пациентов с ХСНсФВ старшего возраста.
Материал и методы
Было проведено открытое сравнительное интервенционное исследование. Отбор пациентов в исследование проводился на амбулаторном приеме в ГБУЗ “Диагностический клинический центр № 1” Департамента здравоохранения города Москвы.
Критерии включения: амбулаторные пациенты в возрасте 60 лет и старше с ХСН IIа–III стадии, II–IV функционального класса (ФК); оптимальная визуализация сердца при двухмерной эхокардиографии (ЭхоКГ); добровольное письменное согласие на участие в исследовании.
Критерии исключения: инфаркт миокарда, острое нарушение мозгового кровообращения в течение 3 мес до включения в исследование; гемодинамически значимые поражения клапанного аппарата сердца; гипертрофическая кардиомиопатия; тахисистолическая форма фибрилляции предсердий (ФП); значительное расхождение конечно-диастолического объема (КДО) ЛЖ и конечно-систолического объема (КСО) ЛЖ при проведении ЭхоКГ с использованием бипланового метода; цирроз печени класса C по классификации Чайлда–Пью; хроническая болезнь почек (ХБП) стадии С5 (скорость клубочковой фильтрации (СКФ) <15 мл/мин/1,73 м2); госпитализации по причине декомпенсации ХСН в течение 3 мес до включения в исследование; изменения в классах медикаментозной терапии в течение 1 мес до включения в исследование.
В исследование было включено 54 пациента, которых разделили на 2 группы в зависимости от приема фозиноприла
(Фозинапа)
или эналаприла в составе рекомендованной общепринятой терапии ХСН [11]:
– основная группа – 29 пациентов, принимающих фозиноприл (Фозинап): 9 мужчин (31%) и 20 женщин (69%) в возрасте 76
(73; 80) лет;
– группа сравнения – 25 пациентов, принимающих эналаприл: 7 мужчин (28%) и 18 женщин (72%) в возрасте 74 (71; 80)
лет.
Фозиноприл (Фозинап) был рекомендован к применению начиная с дозы 10 мг 1 раз в сутки (при необходимости 2 раза в сутки) с постепенным титрованием дозы до 40 мг под контролем клинического состояния, уровня артериального давления (АД), частоты сердечных сокращений (ЧСС). Минимальная доза составила 10 мг, максимальная – 20 мг, средняя – 15,9 ± 5,0 мг/сут. Минимальная доза эналаприла составила 10 мг, максимальная – 20 мг, средняя – 16,4 ± 4,9 мг/сут. Период наблюдения составил 6 мес.
Измерение АД проводилось врачом-исследователем на каждом визите в положении сидя в состоянии покоя после 10-минутного отдыха методом тонов Короткова в количестве 3 раз с помощью профессионального механического тонометра комбинированного типа Little Doctor LD-91 (Little Doctor International (S) Pte. Ltd., Республика Сингапур). Интервал между 1-м и 2-м измерениями составлял не менее 3 мин, между 2-м и 3-м – не менее 10 мин. Артериальное давление на приеме рассчитывали, как полусумму 2-го и 3-го измерений, результаты 1-го измерения не учитывались. Контроль ЧСС проводился врачом-исследователем на каждом визите методом оценки пульса на лучевых артериях в течение 15 с с последующей оценкой наличия дефицита пульса с одновременной пальпацией лучевой артерии и постановкой головки стетофонендоскопа в область верхушечного толчка.
У всех пациентов при включении в исследование осуществлялся сбор жалоб и анамнеза, проводился физикальный осмотр, оценивалась тяжесть клинического и функционального состояния. Тяжесть состояния оценивалась с помощью шкалы оценки клинического состояния (ШОКС). Верификация и лечение ХСН проводились в соответствии с рекомендованными критериями и алгоритмами [11].
Cогласно рекомендациям Американской ассоциации эхокардиографии и Европейского общества сердечно-сосудистой
визуализации, ЭхоКГ выполнялась в двухмерном режиме (В-режиме) на аппарате General Electric Vivid 3. У пациентов с
ФП
оценка ЭхоКГ-параметров проводилась как минимум в 5 последовательных циклах с одинаковой ЧСС.
Индекс глобальной функции (ИГФ) ЛЖ (в %) рассчитывался по формуле:
ИГФ ЛЖ = УО ЛЖ/[0,5 × (КДО ЛЖ + + КСО ЛЖ) + (ММЛЖ/1,05)] × 100,
где УО – ударный объем, ММЛЖ – масса миокарда ЛЖ, которая рассчитывалась по формуле
ММЛЖ = 0,8 × 1,04 × [(МЖП + + ЗСЛЖ + КДР)3 – КДР3 ] + 0,6,
где МЖП – толщина межжелудочковой перегородки, ЗСЛЖ – толщина задней стенки ЛЖ, КДР – конечно-диастолический
размер
ЛЖ. Индекс ММЛЖ рассчитывали как отношение ММЛЖ к площади поверхности тела, определяемой по формуле Дюбуа и Дюбуа
[12].
Статистический анализ данных проводился с использованием программы IBM SPSS Statistics v. 23.0. Качественные переменные представлены в виде частот и процентов, непрерывные количественные данные при нормальном распределении (по критерию Шапиро–Уилка значение p > 0,05) – в виде среднего значения ± стандартное отклонение, при ненормальном распределении – в виде медианы и межквартильного размаха.
При сравнении количественных признаков между 2 независимыми выборками использовался двухвыборочный Т-критерий при нормальном распределении переменных и равенстве дисперсий выборок, в остальных случаях – непараметрический U-критерий Манна–Уитни. При сравнении количественных признаков 2 связанных выборок использовался парный Т-критерий Стьюдента при нормальном распределении разности парных значений изучаемой переменной, в остальных случаях – непараметрический парный критерий Вилкоксона. При сравнении качественных признаков проводился анализ таблиц сопряженности по критерию χ2 Пирсона с поправкой Йейтса и точному критерию Фишера. Различия считали статистически значимыми при двустороннем p < 0,05.

Проведение исследования одобрено этическим комитетом ФГАОУ ВО “Российский национальный исследовательский медицинский университет им. Н.И. Пирогова” Минздрава России
Результаты
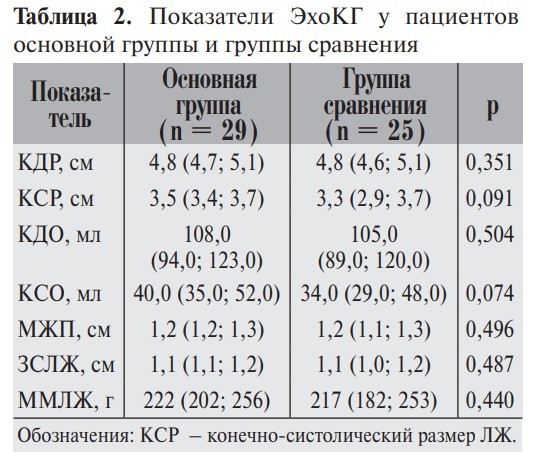
Клинико-демографические показатели пациентов с ХСН основной группы и группы сравнения представлены в табл. 1. Показатели ЭхоКГ представлены в табл. 2.
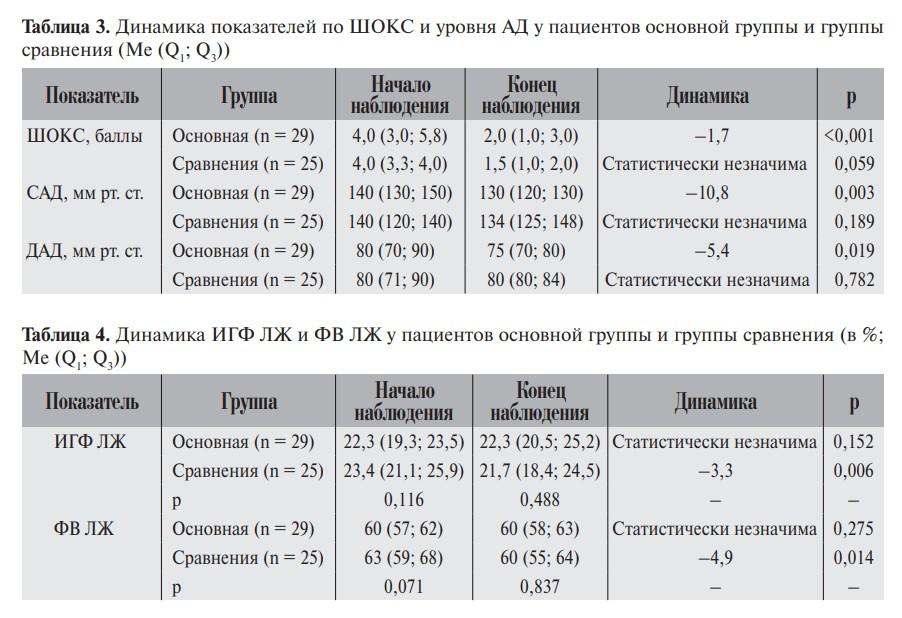
>Комплексное лечение, включавшее препарат Фозинап, привело к cтатистически значимому улучшению клинического состояния, что выражалось уменьшением количества баллов по ШОКС, снижением уровня диастолического АД (ДАД) и систолического АД (САД) (табл. 3). Динамика изменения ЧСС была статистически незначимой как в основной группе (р = 0,626), так и в группе сравнения (p = 0,935). Изменение значений ИГФ ЛЖ и ФВ ЛЖ в процессе лечения представлено в табл. 4.
Статистически значимых изменений других показателей ЭхоКГ в основной группе и группе сравнения зарегистрировано не было.;
За период наблюдения статистически значимого изменения уровня калия зафиксировано не было: основная группа: в начале наблюдения – 4,8 (4,3; 5,1) ммоль/л, в конце наблюдения – 4,4 (4,0; 5,1) ммоль/л (p = 0,652); группа сравнения: в начале наблюдения – 4,7 (4,3; 5,2) ммоль/л, в конце наблюдения – 4,7 (4,1; 4,9) ммоль/л (p = 0,735).
Аналогичные результаты были получены и при оценке уровня креатинина: основная группа: в начале наблюдения – 104 (84; 114) мкмоль/л, в конце наблюдения – 102 (90; 109) мкмоль/л (по критерию Вилкоксона p = 0,938); группа сравнения: в начале наблюдения – 95 (80; 120) мкмоль/л, в конце наблюдения – 88 (66; 139) мкмоль/л (p = 0,848). В основной группе средняя СКФ составила 49 (44; 64) мл/мин/1,73 м2 , в группе сравнения – 57 (47; 66) мл/мин/1,73 м2 (p = 0,429). Отмечено отсутствие динамики СКФ как в основной группе (по критерию Вилкоксона p = 0,955; по критерию знаков p = 1,000), так и в группе сравнения (p = 0,479).
Жалобы на нежелательные явления в виде кашля, который не повлек за собой отмену препарата, предъявляли только 1 некурящая пациентка (3,4%) в возрасте 72 лет с АГ и сахарным диабетом 2-го типа, принимавшая Фозинап, и 1 пациентка (4%) с ишемической болезнью сердца, АГ и ФП, принимавшая эналаприл.
Обсуждение
Результаты проведенного исследования свидетельствуют о более высокой эффективности препарата Фозинап (средняя доза 15,9 мг/сут) в составе комплексной медикаментозной терапии пациентов (медиана возраста 76 лет) с ХСНсФВ II ФК (в среднем 60%) по сравнению с эналаприлом. У 97% пациентов имелась АГ, у 59% – ХБП, у каждого 2-го пациента – ишемическая болезнь сердца в анамнезе и другие патологии, выраженность клинического состояния по ШОКС соответствовала 4 баллам (II ФК по NYHA (New York Heart Association – НьюЙоркская ассоциация кардиологов)). Группу сравнения составили лица аналогичного возраста (р = 0,205) и пола (р = 0,809) с ХСН II ФК, имевшие сопоставимые с основной группой сопутствующую патологию и тяжесть клинического состояния. Клинические параметры пациентов, включенных в исследование, отражают особенности фенотипа пациентов с ХСН, наблюдающихся в амбулаторных условиях в настоящее время, среди которых превалируют лица старшего возраста, с ХСНсФВ и сопутствующей патологией, в основном с АГ, ХБП, ФП, в связи с чем вопрос о рациональной и безопасной комплексной терапии весьма актуален [13].
При выборе тактики лечения пациентов с ХСНсФВ большое значение придается своевременному скринингу и лечению сопутствующих заболеваний. Основные терапевтические направления касаются контроля симптомов, гемодинамической и объемной разгрузки сердца за счет снижения преднагрузки и постнагрузки. Рекомендовано назначение ИАПФ/антагонистов рецепторов ангиотензина II, сакубитрила/валсартана, b-адреноблокаторов, антагонистов альдостерона с целью снижения риска госпитализаций, связанных с обострением ХСН. Терапия диуретиками показана при застойных явлениях для уменьшения выраженности клинических симптомов [11].
Включение в комплексную терапию препарата Фозинап способствовало улучшению клинического состояния пациентов основной группы в виде снижения количества баллов по ШОКС (p < 0,001), лучшего контроля уровня ДАД (р=0,019) и САД (р=0,003), чего не наблюдалось в группе сравнения. Полученные результаты соответствуют данным других исследований, подтверждающим благоприятное влияние фозиноприла на клиническое состояние пациентов с ХСН в виде повышения толерантности к физической нагрузке и снижения ФК ХСН [14, 15].
В российском многоцентровом исследовании ФАСОН (Фармакоэкономическая оценка использования ИАПФ в амбулаторном лечении больных с сердечной недостаточностью) принимали участие пациенты с ХСН (55,6% мужчин) в возрасте старше 60 лет (средний возраст 62 года), которым в составе комплексной терапии назначался фозиноприл в средней дозе 14,7 мг/сут. Была отмечена положительная динамика клинического состояния пациентов (уменьшение показателя по ШОКС с 6,8 до 3,2 балла; р > 0,001), увеличение на 80,2 м расстояния, пройденного в тесте с 6-минутной ходьбой, и повышение ФВ ЛЖ на 4,9%. Затраты на лечение пациентов с ХСН фозиноприлом уменьшились на 54% за счет профилактики декомпенсации сердечной деятельности и госпитализаций [16].
Улучшение контроля АД на фоне лечения фозиноприлом также является существенным аспектом, поскольку неконтролируемая АГ вызывает настороженность из-за усугубления тяжести клинического состояния пациента, снижения качества жизни и ассоциации с неблагоприятным прогнозом. Тем более что согласно результатам наблюдательного исследования ЭПОХА-ХСН, АГ выявляется у 94% лиц с ХСН [17].
В связи с тенденцией к нарушению функции почек и развитию ХБП в старшем возрасте предпочтение следует отдавать ИАПФ с двойным механизмом элиминации из организма – ЖКТ и почки, к которым относится и фозиноприл. На фоне лечения фозиноприлом не наблюдалось изменений СКФ как в основной группе (p = 0,955), так и в группе сравнения (p = 0,479), а также изменений уровня креатинина и калия, что является существенным достоинством этого препарата. Гиперкалиемия – нередкий побочный эффект терапии ИАПФ. Важными факторами, способствующими развитию гиперкалиемии, являются расчетная СКФ 4,5 ммоль/л на фоне приема оптимальной дозы диуретика для данной функции почек. В таких условиях гиперкалиемия является нередким осложнением терапии ИАПФ и служит причиной прекращения лечения или же основанием для применения субоптимальных доз лекарственных препаратов [18].
В 2001 г. в исследовании ESPIRAL была продемонстрирована нефропротективная способность фозиноприла, а спустя 15 лет R. Huang et al. подтвердили этот эффект, показав превосходство фозиноприла над другими антигипертензивными препаратами в комбинации с амлодипином и при монотерапии [19, 20]. Ингибиторы АПФ, включая фозиноприл, в большей степени способствуют дилатации эфферентных, а не афферентных артериол, что приводит к уменьшению внутриклубочкового давления, протеинурии, улучшению кровотока в почках и повышению CКФ. В результате изменений гемодинамики усиливается натрийурез, снижается синтез альдостерона, увеличивается нефропротективный эффект ИАПФ [21].
Фозиноприл образует активный метаболит фозиноприлата, циркулирующий в связанном с белками плазмы крови состоянии (>95%), с периодом полувыведения примерно 12–15 ч, что позволяет рекомендовать прием этого препарата однократно в сутки. При снижении функции почек период полувыведения колеблется от 14 до 32 ч, но накопления препарата не наблюдается. Фозиноприл обладает высоким сродством к липидам (индекс липофильности фозиноприлата превышает 2,0 ЕД) и благодаря этому свойству хорошо проникает через клеточные мембраны и подавляет активность не только циркулирующей, но и тканевой ренин-ангиотензиновой системы в сердце, легких, почках, сосудистой стенке [10, 21].
В исследовании PHYLLIS (The Plaque Hypertension Lipid-Lowering Italian Study) была доказана способность фозиноприла замедлять развитие атеросклероза сонных артерий и предотвращать увеличение комплекса интима–медиа сосудистой стенки у больных АГ с бессимптомным атеросклеротическим поражением каротидного бассейна [22]. Эти результаты согласуются с ранее представленными F. Zonnad et al. данными, согласно которым фозиноприл в сравнении с другими ИАПФ обладает высокой клинической эффективностью и способен замедлять прогрессирование ХСН, реже вызывает ортостатическую гипотензию (р < 0,05), что особенно важно у лиц пожилого и старческого возраста [23].
Патологическое ремоделирование ЛЖ (концентрическое ремоделирование, эксцентрическая и/или концентрическая гипертрофия), которое происходит при ХСН, тесно ассоциировано с активацией нейрогуморальных и иных систем, усугубляющейся при нарушении гемодинамики и повреждении миокарда. Поскольку ФВ ЛЖ полноценно не отражает ремоделирование ЛЖ, включая динамику ММЛЖ, большой интерес представляет ИГФ ЛЖ – маркер, объединяющий функциональные и структурные характеристики ЛЖ в один интегральный показатель. Этот параметр лучше отражает ремоделирование и производительность ЛЖ, поскольку учитывает компенсаторные изменения как объема, так и массы миокарда, что обусловливает его превосходящую прогностическую роль по сравнению с ФВ ЛЖ, нечувствительной к изменениям ММЛЖ [24].
Согласно полученным нами данным, в группе сравнения было отмечено статистически значимое снижение ИГФ ЛЖ (в среднем на 3,3%; p = 0,006) и ФВ ЛЖ (в среднем на 4,9%; p = 0,014) через 6 мес от начала терапии. В основной группе статистически значимая динамика изменений ИГФ ЛЖ и ФВ ЛЖ не была зарегистрирована, что может свидетельствовать о более выраженном кардиопротективном эффекте фозиноприла (Фозинап) по сравнению с эналаприлом за счет избирательного влияния на кардиомиоциты, подавления фиброза и уменьшения ММЛЖ, что проявляется улучшением структурно-функциональных параметров сердца. Этот эффект объясняется многообразием действия АПФ. Помимо регуляции функционирования сердечно-сосудистой системы АПФ является активным участником метаболизма многих биологически активных белков, в частности эндогенного горалатида AcSDKP (N-acetyl-seryl-aspartyl-lysyl-proline) – регулятора пролиферации фибробластов и коллагена в сердце [25].
Побочные эффекты ИАПФ включают сухой кашель, артериальную гипотонию, гиперкалиемию, головокружение и нарушение функции почек, которые чаще возникают у пациентов с более тяжелым клиническим состоянием или получающих лечение несколькими классами препаратов. Пациенты, включенные в наше исследование, не предъявляли жалоб на артериальную гипотонию или головокружение. Это можно объяснить тем, что Фозинап (фозиноприл) обладает двойным путем выведения и реже других ИАПФ вызывает побочные эффекты. Сухой кашель при приеме фозиноприла беспокоил 1 никогда не курившую пациентку, у которой в анамнезе имелись АГ и сахарный диабет 2-го типа, что согласуется с современными представлениями о частоте встречаемости этого побочного эффекта.
Приведенные данные подтверждают гипотезу, что частоту кашля нельзя считать классовым эффектом для ИАПФ, в связи с чем целесообразно переходить с одного препарата на другой. В частности, фозиноприл реже других ИАПФ вызывал кашель (0,8 против 3,6%) и другие побочные эффекты [26, 27].
Заключение
Результаты проведенного исследования свидетельствуют об эффективности и хорошей переносимости препарата Фозинап (фозиноприл) в составе комплексной медикаментозной терапии амбулаторных пациентов с ХСНсФВ II ФК старшего возраста, что проявлялось улучшением их клинического состояния и гемодинамических показателей. На фоне лечения препаратом Фозинап (фозиноприл) не было выявлено изменений СКФ, уровня креатинина и калия, а также ряда ЭхоКГ-параметров, включая ИГФ ЛЖ и ФВ ЛЖ. Хорошие переносимость и профиль безопасности, а также двойной путь выведения из организма являются преимуществами данного препарата, что позволяет рассматривать Фозинап в качестве препарата выбора при лечении мультиморбидных пациентов ХСНcФВ в возрасте 60 лет и старше. Период наблюдения 6 мес является ограничением исследования, что не позволило в полной мере оценить эффекты Фозинапа. Конфликт интересов. Все авторы заявляют об отсутствии конфликта интересов.
